肺がんは、世界中で最も一般的かつ致死率の高いがんの一つであり、進行段階では治療の選択肢が限られているのが現状です。GLOBOCAN 2020のデータによると、肺がんは世界で年間約220万人の新規症例と180万人の死亡者を出しており、がん関連死の筆頭となっています。既存の化学療法、放射線療法、手術といった治療法には、重篤な副作用、長期的な有効性の限界、そして非小細胞肺がん(NSCLC)における頻繁な薬剤耐性といった課題が立ちはだかっています。
このような背景から、新たな補助的治療戦略が切実に求められています。近年、大麻草(Cannabis sativa)由来の非精神活性成分であるカンナビジオール(CBD)が、その潜在的な抗腫瘍効果により、腫瘍学の分野で大きな注目を集めています。本記事では、2025年に発表された最新の系統的レビューに基づき、CBDが肺がん治療においてどのような役割を果たす可能性があるのか、そのメカニズムから臨床的証拠、課題までを詳しく解説します。
カンナビジオール(CBD)とは:THCとの違いと安全性
大麻草には100種類以上のカンナビノイドが含まれていますが、CBDはその中で最も治療への応用が期待されている成分です。
非精神活性: 主な精神活性成分であるΔ9-テトラヒドロカンナビノール(THC)とは異なり、CBDには「ハイ」になるような精神変容作用はありません。
高い安全性: 世界保健機関(WHO)も、CBDは一般的に良好な耐性があり、依存性がないことを認めています。
良好な安全性プロファイル: 重篤な副作用が少なく、臨床での使用においてTHCよりも受け入れられやすい特性を持っています。
これらの特徴が、肺がん治療、特に非小細胞肺がん(NSCLC)におけるCBDの研究を後押しする強い根拠となっています。
CBDが肺がんに作用する「3つの主要メカニズム」
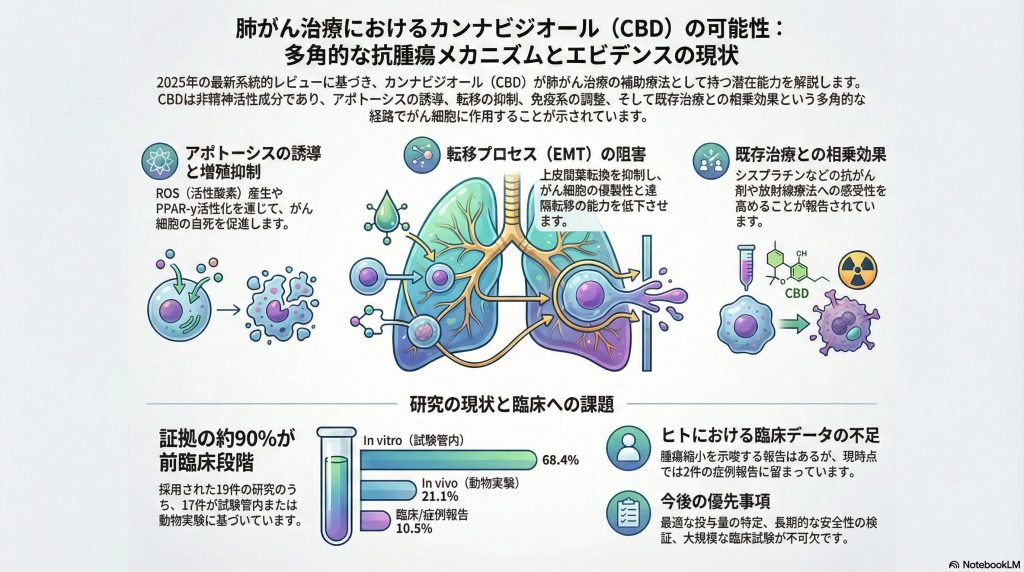
最新の研究では、CBDが複数の経路を通じて肺がん細胞を攻撃することが明らかになっています。主に以下の3つのメカニズムが重要視されています。
① アポトーシス(細胞死)の誘導
CBDは、がん細胞に自死(アポトーシス)を命じる複数の経路を活性化します。
ミトコンドリア機能不全と活性酸素(ROS)の生成: CBDはがん細胞内のミトコンドリアにダメージを与え、酸化ストレス(ROS)を増大させることで、細胞死を引き起こします。
PPAR-γの活性化: 細胞内の受容体であるPPAR-γを活性化し、これがアポトーシス関連タンパク質の働きを強めることが示されています。
がん幹細胞への攻撃: 治療抵抗性や再発の原因となる「がん幹細胞」に対しても、その自己複製能力を低下させ、細胞死を誘導する効果が報告されています。
② 上皮間葉転換(EMT)の抑制と転移の阻害
肺がんの悪性度を高める要因の一つに、細胞が移動・浸潤能力を獲得する「上皮間葉転換(EMT)」があります。
転移の抑制: CBDは、E-カドヘリン(上皮マーカー)の発現を維持し、N-カドヘリンやビメンチン(間葉マーカー)の発現を抑えることで、EMTを食い止めます。
侵襲性の低下: EGFR、MMP-9、FAKといった、がん細胞の浸潤に関わるシグナル伝達を抑制し、がんが他の臓器へ広がるのを防ぐ可能性が示唆されています。
③ 腫瘍免疫微小環境の調節
がん細胞は周囲の免疫環境を操作して攻撃を逃れますが、CBDはこれを正常化する手助けをします。
免疫細胞の活性化: CBDは、腫瘍を攻撃するCD8+ T細胞やナチュラルキラー(NK)細胞の活性を高めることが示されています。
免疫抑制の解除: PD-1/PD-L1シグナル伝達などの、がんによる免疫抑制効果を弱める働きが期待されています。
既存治療との相乗効果:化学療法や放射線療法の「ブースター」として
CBDの最も臨床的に重要な側面は、単独での効果よりも、既存の標準治療を強化する能力にあるかもしれません。
化学療法剤(シスプラチン)への感作: CBDは、薬剤耐性を持つ非小細胞肺がん細胞において、シスプラチンの取り込みを増やし、DNA損傷を促進することで、治療効果を高めることが示されています。
放射線療法の感受性向上: 放射線治療とCBDを併用することで、腫瘍細胞の殺傷効率が上がり、生存率が改善したという動物モデルの報告もあります。
このように、CBDは単体での治療薬というよりは、「補助療法(アドジャンクト)」としての位置づけが有力視されています。
現在の研究データ:期待と現実のギャップ
今回の系統的レビューでは、2007年から2025年までに行われた19の研究が精査されました。その内訳は以下の通りです。
試験管内研究(in vitro): 13件(全体の約70%)
動物実験(in vivo): 4件(全体の約20%)
臨床報告(ヒト): 2件(全体の約10%)
ここで注目すべきは、証拠の90%近くが実験室段階(細胞やマウス)のものであるという点です。前臨床段階のエビデンスは非常に強固で再現性もありますが、ヒトでの有効性を証明する大規模なランダム化比較試験(RCT)はまだ行われていません。
臨床における2つの劇的な症例報告:
ヒトに関するデータは限られていますが、非常に興味深い2つのケーススタディが紹介されています。
76%の腫瘍縮小: 従来の治療を拒否した肺がん患者が2.5年間にわたりCBDオイルを自己投与した結果、腫瘍が76%縮小した例が報告されています。https://pmc.ncbi.nlm.nih.gov/articles/PMC8559110/
部分的な腫瘍退縮: 約1ヶ月間のCBDオイル投与後に、腫瘍の部分的な退縮が見られた別の症例もありますhttps://www.greenzonejapan.com/2019/03/18/cbd_lungcancer/
これらは「仮説を生み出す」という意味で非常に重要ですが、あくまで個人的な経験則(逸話的証拠)であり、これだけでCBDに肺がんを治す力があると断定することはできません。
実用化に向けた課題と注意点
CBDの将来性は明るいものの、臨床現場で一般的に使用されるまでには、解決すべき重要な課題がいくつも残っています。
用量の不一致: 細胞実験では1–10 µM、動物では5–10 mg/kg、ヒトの症例報告では1日200–600 mgと、最適な投与量が確立されていません。
薬剤相互作用: CBDは肝臓の酵素(シトクロムP450)を介して他の薬剤の代謝に影響を与える可能性があり、多く薬を服用する肺がん患者にとっては、安全性の慎重な評価が必要です。
規制の壁: 米国FDAは特定の精製CBD製剤を承認していますが、EUでは「ノベルフード(新規食品)」に分類されるなど、国によって扱いが異なり、臨床開発の妨げとなっています。
研究の質のばらつき: 多くの前臨床研究で、盲検化やランダム化の報告が不十分であり、さらなる厳格な検証が求められています。
結論:私たちはどう向き合うべきか?
現段階において、CBDは肺がん治療における「有望な調査段階の補助療法」と見なすべきです。
前臨床試験で見られるアポトーシス誘導、転移抑制、免疫調節といった多面的な作用は非常に魅力的です。特に、シスプラチンなどの化学療法や放射線療法の効果を高める可能性は、治療の行き詰まりを感じている患者にとって大きな希望となります。
しかし、「臨床的な証拠はまだ不十分」であることを忘れてはなりません。医師の指導なしに自己判断で標準治療を置き換えることは推奨されません。今後の研究で、適切な用量、長期的な安全性、そしてどのようなタイプの患者が最も恩恵を受けられるか(バイオマーカーの特定)が明らかになることが期待されます。
将来的には、ナノ製剤や吸入器を用いた新しい投与方法により、肺組織への直接的なデリバリーが可能になるかもしれません。CBDが肺がん治療の標準的な一部となるためには、今後行われるであろう大規模なヒト臨床試験の結果を待つ必要があります。
まとめ: CBDは肺がん細胞の弱点を多角的に突く科学的に興味深い候補ですが、現時点ではあくまで「将来が期待される補助的な選択肢」です。今後の厳格な検証を経て、肺がん患者の生存率とQOL(生活の質)を改善する新たな武器となることが期待されます。
参考文献:https://pubmed.ncbi.nlm.nih.gov/41126219/
執筆: 正高佑志 Yuji Masataka(医師) 経歴: 2012年医師免許取得。2017-2019年熊本大学脳神経内科学教室所属。2025年聖マリアンナ医科大学・臨床登録医。研究分野:臨床カンナビノイド医学 活動: 2017年に一般社団法人Green Zone Japanを設立し代表理事に就任。独自の研究と啓発活動を継続している。書籍: お医者さんがする大麻とCBDの話(彩図社)、CBDの教科書(ビオマガジン) 所属学会: 日本内科学会、日本臨床カンナビノイド学会(副理事長)、日本てんかん学会(評議員)、日本アルコールアディクション医学会(評議員) 更新日:2026年4月1日




コメントを残す