令和6年度厚生労働科学特別研究事業「カンナビノイド医薬品とカンナビノイド製品の薬事監視」の一環として行った『先進6カ国における未承認大麻製剤の処方制度』に関する調査報告の第2弾です。
※ 先進6カ国とは厚生労働省が定義するもので、アメリカ・カナダ・オーストラリア・イギリス・ドイツ・フランスです。このうち、国として医療大麻制度を運用しているのは(2025年3月時点で)カナダ・オーストラリア・イギリス・ドイツの4カ国でした。このブログでは、この4カ国のそれぞれについて、4回に分けて紹介しています。第2回目はオーストラリアです。
海外の医療大麻制度 [ 1 ] カナダ
海外の医療大麻制度 [ 3 ] イギリス
研究要旨 【目的】厚生労働省の定める先進6カ国(アメリカ・カナダ・オーストラリア・イギリス・ドイツ・フランス)のうち、処方箋医薬品として認可されていない大麻製剤を医師が患者に処方することが合法である国について、その制度設計および処方の実態を調査し、日本における制度設計の際の参考とする。 【方法】市場調査会社が公表しているデータ、および各国の業界関係者に聞き取りを行った。イギリスについては実際に足を運び、関係者に話を伺った。 【結果】現在、未承認大麻製剤が合法的に処方されているのは、上述の6カ国のうち、カナダ・オーストラリア・イギリス・ドイツの4カ国である。各国の制度の詳細については本文にて詳述する。 【考察】各国で制度は異なるが、処方箋医薬品でもなく健康補助食品でもない「医療用大麻製剤」というカテゴリーが存在し、医療関係者の合法的な処方のもとに使用している患者がいるという事実は共通している。本邦においても、同様の大麻製剤の使用が認められることによって恩恵を得られる潜在的な患者は多数にのぼると考えられ、日本の医療制度や患者の実情に則した制度が制定されることが望ましい。
オーストラリアの医療大麻制度
1. 法的枠組み
2016年に「麻薬取締法1967(Narcotic Drugs Act 1967)」(1) および「治療用物品管理法 1989(Therapeutic Goods Administration Act 1989)」(2) が改定され、医療目的での大麻の栽培、生産、処方が合法化された。これにより、医療目的での大麻製剤の使用が特定の条件下で認められるようになった。(注記:オーストラリアでは現在も嗜好目的の大麻は禁じられている。)
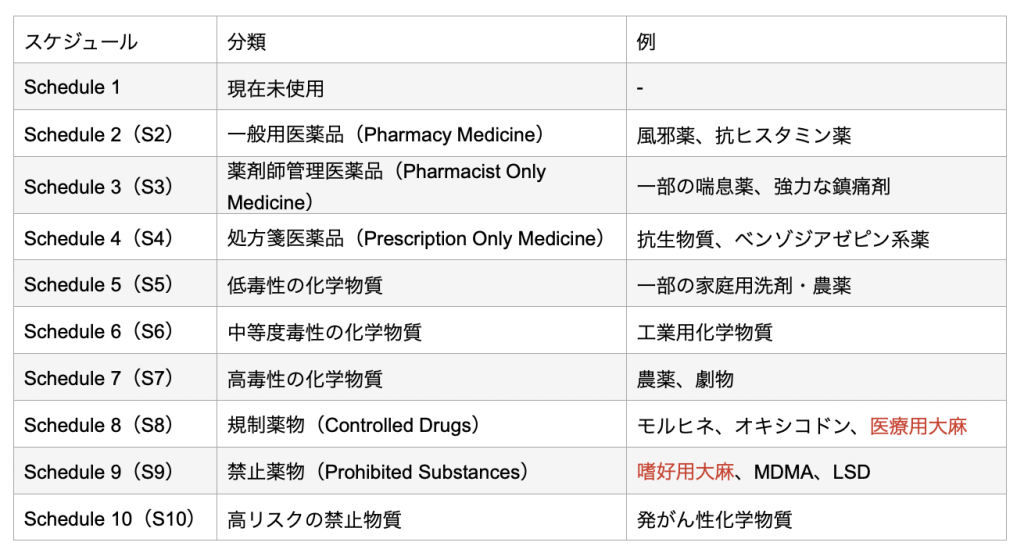
「麻薬取締法1967」は規制の対象となる薬物を「麻薬(narcotic drugs)」と「向精神薬(psychotropic substances)」に分類しており、大麻は「麻薬」である。また保健省医療用品管理局(Therapeutic Goods Administration, TGA)(3) は、オーストラリアにおいて医薬品や毒物を管理するための基準である「Poisons Standard」(正式名称は “Standard for the Uniform Scheduling of Medicines and Poisons, SUSMP)(4) を管轄しており、薬物をスケジュール 1 から 10 に分類して管理している。このなかで、医療用大麻はスケジュール8の規制薬物(Controlled Drug)、嗜好用大麻はスケジュール9の禁止薬物(Prohibited Substances)に分類されている。
医療大麻制度の運用は、保健省医療用品管理局によって行われている。TGAは、未承認大麻製剤の品質と安全性の確認、大麻製剤へのアクセス、臨床試験の監督、研究データの活用、医療従事者と患者への情報提供、規制の施行と監視に責任を持つ。
医療用大麻製剤の輸入・製造の監督は保険省医薬品規制局(Office of Drug Control, ODC)(5)の管轄である。
2. 利用者の資格
処方の対象となる疾患は医師の判断に委ねられるが、一般的には以下のような疾患が対象となる。
慢性疼痛:神経性疼痛およびがん性疼痛
神経疾患:てんかん、多発性硬化症、パーキンソン病、トゥーレット症候群など
精神疾患:PTSD、不安神経症、うつ病など
がんによる悪心や食欲不振
消化器疾患:クローン病、潰瘍性大腸炎、過敏性腸症候群など
緩和医療および終末期医療
その他:自閉症、線維筋痛症、睡眠障害、頭痛・片頭痛、関節炎など
3. 利用の手順
製品の輸入、栽培、製造、供給は、医療用品管理局(TGA)および医薬品規制局(ODC)が監督している。国内での医療用大麻の栽培は、ODCによって厳密に規制されており、許可を受けた企業が、医療品質基準に従って大麻を栽培および製造する。 一部の製品は、カナダやオランダなどから輸入されることもある。医療大麻患者が自身の使用のために大麻を栽培することは許されていない。
まず、患者が大麻製剤を入手する手順の概略は以下の通りである。
① 医療従事者による診察により、医療大麻製剤の使用が適切であるかどうかの判断を受ける。
② 使用の許可を受ける。
③ 医療従事者が個々の患者の症状に合わせた処方箋を書く。医療大麻の処方を行えるのは医師(一般開業医 [GP] または専門医)およびナース・プラクティショナーのみである。
④ 患者は処方箋を持参して認可された薬局から医療大麻製品を購入するか、処方箋を薬局に送付し、製品を自宅に配送してもらう。
⑤ 患者は定期的に医療従事者の診察を受け、大麻製剤の効果を監視し、必要ならば製品や用量を調整する
次に、②の、患者が使用の許可を受ける方法について詳述する。患者が医療用大麻製剤の使用許可を受ける方法には、「特別アクセススキーム」と「認定処方医制度」の2つがある (6) (7)。
A: 特別アクセススキーム(Special Access Scheme, SAS)
医療従事者が患者に代わって個別に、TGAに処方の許可を申請する方法である。SASにはカテゴリーAとカテゴリーBがあり、その違いは以下の通り。
A-1: SAS カテゴリーA
• 重篤な疾患または末期状態にある患者で、「生命が危険にさらされる可能性がある」または「治療がない場合に致命的なリスクが高い」患者が該当する。
• 申請方法:医師が患者の状況を判断し、通知を行った後に製品を処方できる。TGAの事前承認は不要で、申請は後日通知として行う。
• 即時対応が必要な場合に適している。事前審査が不要なため迅速に治療を開始できる。
A-2:SAS カテゴリーB
• 重篤な疾患ではあるが末期状態ではなく、カテゴリーAに該当しない患者を対象とする。
• 医療大麻を含む未承認医薬品を使用することで健康状態が改善する可能性がある場合が該当する。
• 申請方法:医師が患者のためにTGAに申請し、事前に承認を受ける必要がある。TGAは製品の適応性やリスク・ベネフィットを審査し、承認の可否を決定する。
• 承認プロセスに数日から数週間かかることがあり、緊急性が低い場合や、慎重な審査が求められる場合に適している。
B. 認定処方医制度(Authorised Prescriber, AS)
特定の医療従事者(主に医師だがナース・プラクティショナーも含まれる)が未承認の医療大麻製剤を特定の患者グループに直接処方できるようにする制度である。この制度は、特定の条件下で医師が迅速かつ効率的に未承認医薬品を使用するためのアクセス手段を提供する。以下にその概要を示す。
• 医師はTGAに申請し、認定を受ける。認定のためには下記の要件を満たすことが必要である。
– 適切な資格と経験:処方する医薬品(医療大麻を含む)や治療対象となる疾患に関する専門知識があること。
– 患者の安全を確保する治療計画:処方される医薬品が適切かつ安全に使用されることを示す治療計画を提出すること。
– 倫理委員会(Human Research Ethics Committee, HREC)または専門学会からの承認
• APスキームでは、医師が認定を受けた特定の患者グループ(例: 特定の疾患や症状に苦しむ患者)に対してのみ未承認医薬品を処方できる。患者ごとにTGAの承認を申請する必要はないが、処方状況を定期的に報告する義務があり(通常は6か月ごと)、報告内容には、処方件数や治療結果に関する概要が含まれる。
• 認定は通常1~3年の有効期間があり、更新時には再審査が行われる。
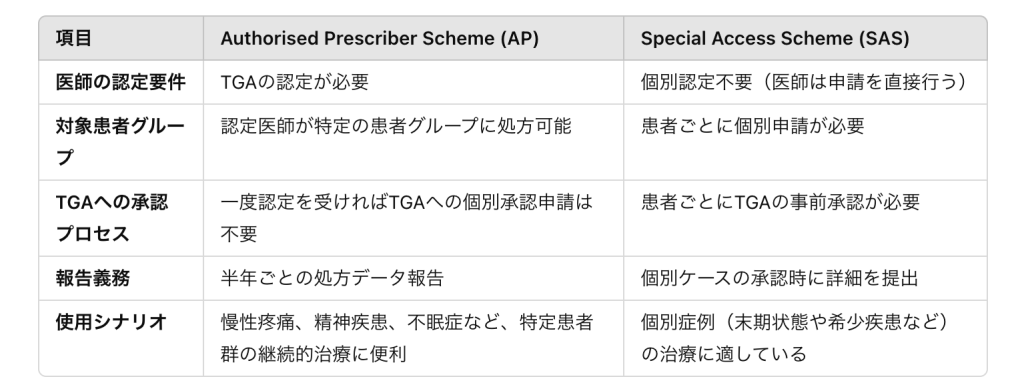
認定処方医制度と特別アクセススキームの違いをまとめると以下の通りである。
“Established History of Use” リストについて
オーストラリアの”Established History of Use”制度はTGAが管理するリストで、未承認医薬品全般のうち、一定の使用実績と安全性が確認された製品をまとめたものである。2025年1月現在、TGAのウェブサイトにあるリスト (8) には168製品が掲載され、このうち18製品が医療大麻製剤である。(注記:掲載されるのは個別のブランド/商品名ではなく、成分比、剤形、適応疾患の組み合わせである。)
このリストに掲載されている医薬品は、TGAが「安全かつ効果的であると十分な歴史的使用実績から判断した」と認めた製品であり、医師がこれらの製品を処方する際、申請プロセスが簡素化される。リストに含まれる製品に関しては、医師と患者が安全性をより信頼でき、かつ医師の処方申請手続き(特にSAS カテゴリーBおよびAPスキーム)がスムーズになるという利点がある。リスト掲載製品は、製造・品質管理基準(例: GMP基準)を満たしている必要があり、TGAが最新の研究や安全性データをもとにリストを定期的に見直す。
4. 流通経路
製品の種類
現在医師が患者に処方できる未承認医療用大麻製剤は、THCとCBDの比率によって5つのカテゴリーに分類されている。医師はこのなかから特定の「カテゴリー」を処方する。
カテゴリー 1: CBD のみ (CBD ≥ 98%) : 63製品
カテゴリー 2: CBD 優位 (CBD ≥ 60% and < 98%):41製品
カテゴリー 3: 含有比拮抗 (CBD <60% and ≥ 40%):51製品
カテゴリー 4: THC 優位 (THC 60% – 98%):15製品
カテゴリー 5: THC のみ (THC >98%):345製品
全製品のリストは保健省のウェブサイトで見ることができる (9)。
申請手続きはすべてオンラインで可能となっている (10)。
医療大麻の輸入規定 (11)
制度が始まった当初は、患者別に申請してその人の分だけ輸入というルールだったが、それではあまりに輸送コストがかかりすぎて高額になってしまうため、製造業者あるいは輸入業者が「スポンサー(SPONSOR)」となってバルクで輸入し、あらかじめ認可された倉庫に保管し、そこから患者あるいは薬局に販売される制度に変更された。
(1) 輸入業者の登録 :輸入業者は、TGAの輸入許可とODCの麻薬許可(Narcotic Import Permit)を取得する必要がある。また製品はGMP基準(Good Manufacturing Practice)に準拠している必要がある。
(2) 未承認医薬品としての取り扱い:オーストラリアでは、医療大麻製品のほとんどが未承認医薬品とみなされており、輸入された製品は、SASまたはAPというアクセス制度の下で、または臨床試験を通じてのみ処方される。
(3) 輸入可能な製品:輸入できる製品は、TGAが承認した特定の医療大麻製品リストに含まれるもの、または個別の承認を受けた製品に限られる。
(4) 輸送と保管の規制:医療大麻製品は、適切な輸送条件(例: 温度管理)で輸送される必要があり、保管には厳格なセキュリティと記録管理が求められる。
スポンサーの役割
医療大麻の輸入におけるスポンサーは、以下のような役割を果たす:
1. 法的責任:スポンサーは輸入された医薬品の規制遵守に対して法的責任を負い、製品がオーストラリアの基準を満たしていることを保証する(例: ラベリング、品質基準)。
2. TGAとの連携:スポンサーは、TGAとのやり取りを通じて、製品の登録または使用許可を取得し、必要に応じて、医療大麻製剤をTGAの「Established History of Use List」に追加する申請を行うこともある。
3. 医師と患者のサポート:スポンサーは、製品の適正使用に関する情報提供を行い、また、医師がSASやAPの申請を行う際に、製品情報や技術的なサポートを提供する場合がある。
4. 製造元との調整:スポンサーは海外の製造元と連携して製品の輸入手続きや供給管理を行い、製品の輸送、税関手続き、流通までの全プロセスを管理する。
スポンサー関与の具体例
例えば、特定の医療用大麻製剤を使用したい場合、以下の流れでスポンサーが関与する:
1. 医療従事者がSASまたはAP経由で患者に処方:医療従事者が特定の製品を選択。
2. スポンサーが輸入と供給を手配:必要な輸入許可を取得し、製品を国内へ。
3. 患者に届けられる:スポンサーのサプライチェーンを通じて、処方薬局または医師のもとへ供給。
上述した、医療用大麻製剤のカテゴリー別製品が網羅されたTGAのウェブサイトページには、各製品のスポンサー名が明記されている (9)。
5. 医療用大麻製剤利用の実態
● 処方する医療従事者の数
2024年の時点でオーストラリアには、約142,500人の医師と2,250人のナース・プラクティショナーがいる (12) (13)。このうち、SAS および AP 制度を通じて医療用大麻製剤を処方する医療従事者は約5,700人とされている (14)。
● 利用者の数
医療用大麻製剤の利用者の数を包括的に管理する機関はなく、正確な数を把握することは困難だが、オーストラリア健康福祉研究所(Australian Institute of Health and Welfare, AIHW)が2022年から2023年にかけて行ったアンケート調査 (15) では、過去12か月間に医療目的で大麻を使用したと回答したのは全国民の3%にあたる約70万人であったのに対し、オーストラリア医療従事者規制庁(Australian Health Practitioner Regulation Agency, AHPRA)およびAPRAがサポートする国家委員会(National Boards)が共同で行った報告 (14) によれば、2024年1月までに、医療目的で大麻を使った経験のある人の数は100万人を超える。これは、医療大麻製剤の利用が急速に拡大していることを示している。
患者の数を使用スキーム別に見ると、スペシャルアクセススキーム(SAS)を通して医療大麻製剤を使っている人の方が認定医師制度(AP)を通して使っている人よりも多く、その大部分を占める。
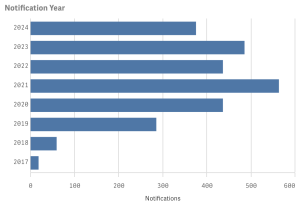
SAS Category A (16)
2016〜2024年の使用報告総数:2,657件
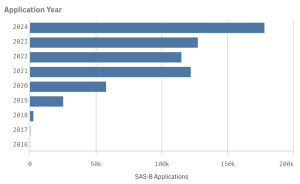
SAS Category B (17)
2016〜2024年の使用許可申請総数:627,600件
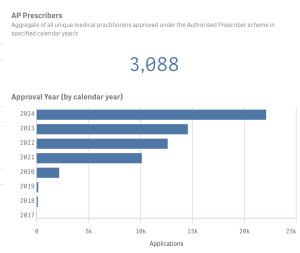
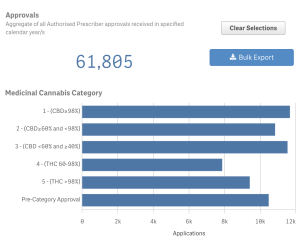
AP (18)
2025年1月27日時点で認定医師の数は3,088名、これまでに認定医師が承認した処方数は61,805件。
● 使用の目的(疾患)
大麻の医療利用が合法化された2016年から2021年8月までの5年間について、その使用の目的をまとめたTGAの報告書 (19)によれば、承認された処方のうち、主要な対象疾患は疼痛管理、不安、睡眠障害がそれぞれ61%、16%、5.7%となっている。
より最近では、2022年〜2023年に行われたアンケート調査の結果が 2024年に発表されており(20)、同じく主要な対象疾患は、疼痛管理37%、精神疾患36%、睡眠障害15%で、上記の結果をなぞっている。
6. 課題
医療用大麻製剤は、承認された医薬品も含め、オーストラリアの公的医療保険制度である「メディケア」(Medicare)(21)および公的な医薬品助成制度である「医薬品給付制度」(Pharmaceutical Benefits Scheme, PBS)(22) の対象ではなく、すべて患者の自費負担となる。一般に大麻製剤は高額であり、患者の負担が大きいことが問題となっている。(唯一の例外として、2021年5月より、ドラベ症候群に限りエピディオレックスがPBSの適応対象となっている 。)(23)
文責:三木直子(国際基督教大学教養学部語学科卒。翻訳家。2011年に『マリファナはなぜ非合法なのか?』の翻訳を手がけて以来医療大麻に関する啓蒙活動を始め、海外の医療大麻に関する取材と情報発信を続けている。GREEN ZONE JAPAN 共同創設者、プログラム・ディレクター。)
<参照文献>
1) Australian Government. Narcotic Drugs Act 1967 (最終更新 2022-02-21). <https://www.odc.gov.au/resources/legislation/narcotic-drugs-act-1967> Accessed March 2025.
2) Australian Government. Therapeutic Goods Act 1989 (最終更新 2024-10-14). <https://www.legislation.gov.au/C2004A03952/latest/text> Accessed March 2025.
3) Australian Government. Therapeutic Goods Administration (TGA) (n.d.). <https://www.tga.gov.au/> Accessed March 2025.
4) Australian Government. The Poisons Standard (the SUSMP) (n.d.). <https://www.tga.gov.au/how-we-regulate/ingredients-and-scheduling-medicines-and-chemicals/poisons-standard-and-scheduling-medicines-and-chemicals/poisons-standard-susmp> Accessed March 2025.
5) Australian Government. Office of Drug Control (n.d.). <https://www.odc.gov.au/> Accessed March 2025.
6) Australian Government. Medicinal cannabis: access pathways and usage data (最終更新 2025-01-28). <https://www.tga.gov.au/products/unapproved-therapeutic-goods/medicinal-cannabis-hub/medicinal-cannabis-access-pathways-and-usage-data#dashboard> Accessed March 2025.
7) Australian Government. Medicinal cannabis Authorised Prescriber Scheme data (最終更新 2024-05-01). <https://www.tga.gov.au/products/unapproved-therapeutic-goods/medicinal-cannabis-hub/medicinal-cannabis-access-pathways-and-usage-data/medicinal-cannabis-authorised-prescriber-scheme-data> Accessed March 2025.
8) Australian Government. Authorised Prescriber established history of use lists (最終更新 2024-01-15). <https://www.tga.gov.au/products/unapproved-therapeutic-goods/prescribe-unapproved-therapeutic-good-health-practitioners/lists-products-established-history-use/authorised-prescriber-established-history-use-lists> Accessed March 2025.
9) Australian Government. Medicinal cannabis products by active ingredients (最終更新2025-03-12). <https://www.tga.gov.au/medicinal-cannabis-products-active-ingredients> Accessed March 2025.
10) Australian Government. Special Access Scheme & Authorised Prescriber Scheme Online System (n.d.). <https://compliance.health.gov.au/sas/> Accessed March 2025.
11) Australian Government. Supply and wholesaling of medicinal cannabis products
(MCP) (April 2021). <https://www.tga.gov.au/sites/default/files/supply-and-wholesaling-medicinal-cannabis-products-mcp.pdf> Accessed March 2025.
12) Australian Health Practitioner Regulation Agency. Medical practice in 2023/24(最終更新2025-02-27). <https://www.medicalboard.gov.au/news/annual-report.aspx> Accessed April 2025.
13) Australian College of Nurse Practitioners. About Nurse Practitioners (n.d.) <https://www.acnp.org.au/about-nurse-practitioners> Accessed March 2025.
14) Australian Health Practitioner Regulation Agency. Regulators come together as one million Australians turn to medicinal cannabis treatments (2024-02-20). <https://www.medicalboard.gov.au/News/2024-02-20-medical-cannabis-treatment.aspx> Accessed April 2025.
15) Australian Government. Medical marijuana/cannabis in the NDSHS (最終更新 2024-02-29). <https://www.aihw.gov.au/reports/medicines/medical-marijuana-cannabis> Accessed March 2025.
16) Australian Government. SAS-A Notifications (n.d.). <https://dashboard-data.health.gov.au/single/?appid=1066afbe-2b37-427d-8c47-2caa5082cccc&sheet=4c57fba1-4b0d-423f-a42e-558bd76d4f21&select=clearall> Accessed March 2025.
17) Australian Government. SAS-B Approvals (n.d.). <https://dashboard-data.health.gov.au/single/?appid=1066afbe-2b37-427d-8c47-2caa5082cccc&sheet=088f611b-10de-4d72-be68-ccf8d12c54e9&select=clearall> Accessed March 2025.
18) Australian Government. Medicinal cannabis Authorised Prescriber Scheme data (最終更新 2024-05-01). <https://www.tga.gov.au/products/unapproved-therapeutic-goods/medicinal-cannabis-hub/medicinal-cannabis-access-pathways-and-usage-data/medicinal-cannabis-authorised-prescriber-scheme-data> Accessed March 2025.
19) MacPhail, Sara, et al. Medicinal Cannabis Prescribing in Australia: An Analysis of Trends Over the First Five Years (2022-05-10). <https://www.frontiersin.org/journals/pharmacology/articles/10.3389/fphar.2022.885655/full> Accessed March 2025.
20) Mills, Llewellyn, et al. Medical cannabis use in Australia seven years after legalisation: findings from the online Cannabis as Medicine Survey 2022–2023 (CAMS-22) (May 2024). <https://harmreductionjournal.biomedcentral.com/articles/10.1186/s12954-024-00992-1> Accessed April 2025.
21) Australian Government. Medicare (n.d.). <https://www.health.gov.au/topics/medicare?language=und> Accessed March 2025.
22) Australian Government. Pharmaceutical Benefits Scheme (PBS) (n.d.). <https://www.pbs.gov.au/pbs/home> Accessed March 2025.
23) Ministers: Department of Health and Aged Care. (2021-04-31). <https://www.health.gov.au/ministers/the-hon-greg-hunt-mp/media/historic-pbs-listing-for-australians-with-a-rare-epilepsy-condition> Accessed April 2025.





コメントを残す